연구소소개
-
26
혈액 검사 없이 침으로 진단하는 콜레스테롤 검출 센서 개발
- 고지혈증 진단에 타액(침)을 이용한 비침습형 콜레스테롤 고감도 분석 기술 개발 - 향후 타액(침) 및 체액(소변, 땀)을 이용한 극미량 바이오마커 검출 응용 기대 현대인의 식습관과 생활방식의 변화로 인해, 비만 및 대사성 질환 환자의 증가는 국민의 건강 뿐 아니라 막대한 국가·사회적 비용을 소모할 정도로 심각한 문제로 야기되고 있다. 따라서 전주기적 조기진단 및 질병 예방을 위해 일상생활에서 손쉽게 진단이 가능한 비침습적 스크리닝 기술 및 자가진단의 필요성이 커지고 있다. 최근 국내 연구진이 사람의 타액(침) 만으로 콜레스테롤을 검출 및 분석할 수 있는 기술을 개발했다고 밝혔다. 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 바이오마이크로시스템 연구단 이수현 박사팀은 혈액 검사 없이 고지혈증과 같은 지질대사 이상 질환자들의 타액(침)에 들어있는 극미량의 콜레스테롤을 분석할 수 있는 고감도 센서 플랫폼을 개발했다고 밝혔다. 타액을 이용한 콜레스테롤 측정 기술은 고지혈증과 같은 질병을 손쉽게 자가 진단할 수 있다. 혈액 검사와 같은 기존 진단법은 침습적 검사법으로 통증으로 인한 스트레스 유발 및 각종 감염의 위험성을 지니는 단점이 지적되었다. 그러나 타액은 시간과 장소에 구애받지 않고 비침습적으로 손쉽게 시료 수집이 가능하고, 혈액 내의 콜레스테롤 같은 각종 바이오마커 농도와 높은 상관관계를 갖기 때문에 타액을 기반으로 하는 비침습적 진단기기 개발 연구들이 활발히 이루어지고 있다. 그러나 타액 내의 콜레스테롤 농도는 혈액 대비 1/100~1/1,000 정도 수준에 불과하기 때문에 이를 위해서는 민감도가 향상된 센서 및 플랫폼 개발이 필수적이었다. KIST 연구진은 만성대사성 질환에 대한 전주기적인 조기진단 및 질환 예방을 위한 새로운 패러다임인 사용자 친화적인 임상진단 기술을 개발하기 위해서 타액의 측정 프로토콜을 정립하고, 기존의 휴대용 혈중 콜레스테롤 기반의 검출 센서에 비해 1,000 배 정도 높은 민감도를 가지는 센서 및 플랫폼을 개발하였다. KIST 이수현 박사팀은 고농도의 콜레스테롤 산화효소를 고정화할 수 있는 나이트로셀룰로스(Nitrocellulose)* 페이퍼와 백금 나노 구조를 갖는 고성능 센서를 각각 제작하여, 결합했다. 이 결합된 센서는 타액 내 극미량(ng/ml, 1ml(밀리미터) 용액 속에 존재하는 ng(나노그램)) 수준의 콜레스테롤을 전기화학적 임피던스** 변화 측정을 통해 검출이 가능하다. 이는 기존에 빛이 흡수하는 정도로 농도를 측정하는 흡광법과 비교시 약 100배 높은 감도이다. 연구진은 제작된 센서로 실제 고지혈증 환자의 혈액 및 타액 샘플을 측정·비교한 결과, 타액 내 존재하는 콜레스테롤의 농도가 혈액 내 농도 대비 약 1/1000 정도 비례하여 낮게 존재하는 것을 확인하였다. *나이트로셀룰로스(Nitrocellulose) : 플래쉬 코튼이라고 불리는 섬유소(셀룰로스) 중합체의 일종 **전기화학 임피던스 측정(Electrochemical impedimetry) : 주파수가 다른 교류신호를 셀에 부여하여 계측하는 측정 방법 KIST 이수현 박사는 “이번 기술은 타액·체액 기반의 각종 호르몬 및 포도당 검출 등에 다양하게 응용될 수 있으며, 혈액 기반 진단 칩 시장에 비해 편의성과 기술적 진보성에서 우위를 점할 것으로 기대된다.”고 연구의의를 밝혔다. 또한 “고지혈증을 비롯한 다양한 지질대사 이상 증세의 보다 정확한 진단과 실용화를 위해서 보다 많은 수의 임상 샘플을 이용한 타액 내 저밀도·고밀도 지질단백질 콜레스테롤 및 중성지방 검출을 위한 추가 연구를 수행할 계획”이라고 밝혔다. 본 연구는 과학기술정보통신부(장관 유영민) 지원으로 한국연구재단 바이오·의료기술개발사업 및 KIST 기관고유사업으로 수행되었으며, 연구결과는 센서 분야 국제학술지인 ‘Sensors and Actuators B: Chemical’ (IF : 5.667, JCR 분야 상위 2.459%) 최신호로 출판되었다. * (논문명) Enzyme-loaded paper combined impedimetric sensor for the determination of the low-level of cholesterol in saliva - (제1저자) 한국과학기술연구원 이이재 선임연구원 - (교신저자) 한국과학기술연구원 이수현 책임연구원 <그림설명> <그림 1> 고지혈증 진단을 위한 타액(침) 내 극미량 콜레스테롤의 비침습적 검출 센서 개발
- 25
- 작성자바이오마이크로시스템연구단 이수현 박사팀
- 작성일2018.10.18
- 조회수12486
-
24
우리 몸 운동능력 조절하는 소뇌, 비신경세포가 소뇌에 관여하는 매커니즘 밝혔다
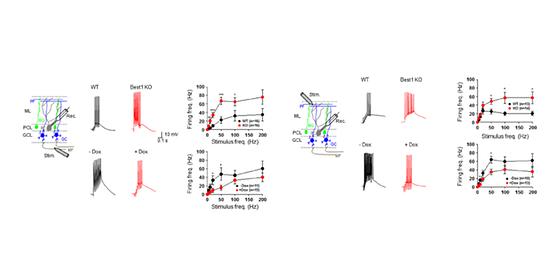
- KIST-단국대 공동연구팀, 비신경세포(별세포) 속 전달물질의 신경활성 조절기능 규명 - 소뇌 운동능력에 직접적 관여, 향후 뇌 손상으로 인한 운동 장애 및 질병 치료 기대 소뇌(Cerebellum)는 우리 몸의 평형유지 등에 관여하는 정밀한 제어기관으로, 운동 능력과 밀접하게 관련이 있다. 따라서 소뇌의 기능저하는 보행, 운동, 손의 움직임 등에 장애를 가져올 수 있고, 안구운동, 언어구사의 문제와도 연결되어있다고 알려져 있다. 이렇듯 소뇌의 신경세포가 손상되거나 신호전달이 이루어지지 않으면 운동신경 및 인지기능에 장애가 올 수 있다. 최근 국내연구진이 소뇌의 운동능력에 관여하는 신경세포의 역할 외에도, 비신경세포에서 나온 억제성 전달물질이 신경세포의 활성을 조절하여 운동 능력에 관여한다고 밝혔다. 한국과학기술연구원(KIST, 원장 이병권) 신경교세포연구단 이창준 박사 연구팀은 단국대학교 윤보은 교수팀과의 공동연구를 통해 뇌의 비신경세포인 ‘별세포’*에서 합성되어 지속적으로 분비되는 ‘가바’**라는 물질이 신경세포의 활성을 조절하고 나아가 운동 능력에 관여하는 것을 세계 최초로 밝혔다. *별세포(Astrocyte) : 신경세포 주변의 비신경세포. 비신경세포(Glia)에서 가장 큰 비중을 차지하는 세포로 뇌와 척수에 존재하는데, 별모양을 하고 있어 별세포라 일컬어진다. 신경세포의 이온농도 조절, 노페물 제거, 식세포작용 역할 **지속적 가바(Tonic GABA) : 신경계의 균형을 유지하는데 중요한 물질. 신호를 전달하는 물질 중 억제성 물질인 가바는 다양한 작용방식으로 분출되는데 그 중 지속적 가바는 비신경세포에서 지속적으로 분비되어 지속적 가바로 불린다. KIST 이창준 박사팀은 소뇌 속의 비신경세포인 별세포가 억제성 신호전달 물질인 가바를 생산하고 분비하는 역할을 하며, 비신경세포에 항상 존재하는 ‘지속적 가바’는 뇌 내 흥분과 억제의 균형 유지에 필수적인 기작으로 소뇌 신경세포의 흥분 정도, 신호전달, 시냅스의 환경에 따른 구조 ·기능적 변화 등을 조절한다는 것을 확인하였다. 또한 동물 행동실험을 통해 이것이 소뇌의 주기능인 운동조절기능에 기여한다는 것을 밝혔다. 연구진은 실험을 통해 실험쥐에게 저해제를 먹여 ‘지속적 가바’의 생산을 감소시킨 쥐와 유전자 변이를 통해 ‘지속적 가바’를 분비하는데 문제가 생긴 쥐는 운동조절이 향상된 반면, ‘지속적 가바’의 생산을 비정상적으로 증가(활성화)시킨 쥐는 운동능력 감소 및 조절기능이 떨어진 것을 확인했다. 또한, ‘지속적 가바’의 생산이 감소된 쥐의 경우 대조군에 비하여 30~60% 까지 운동 능력이 향상되었으며, ‘지속적 가바’가 과잉 증가된 경우에는 대조군에 비하여 운동능력이 40%정도 감소하는 것을 확인할 수 있었다. 본 연구는 KIST 연구진이 사이언스지(2010년), 세계생리학회지(2014년)에 발표한 연구결과에 대한 후속연구로, 선행 연구들을 통해 비신경세포에서 억제성 신경전달물질인 가바가 분비되고, 합성된다는 연구 결과를 발표한바 있다. 연구진은 이를 바탕으로 기존 연구 결과에서 생리적 기능에 대해 보고된 것이 없는 ‘지속적 가바’가 뇌에서 신경세포의 활성과 신호전달에 미치는 영향을 밝혔고, 그것이 운동조절이라는 생리적 역할과 직접적 연관이 있다는 것을 규명하여 비신경세포가 뇌 기능 조절에 중요하게 작용함을 밝혔다. KIST 이창준 박사는 “현재 소뇌의 손상 및 퇴화와 관련된 운동장애는 추가적인 손상을 늦추거나 장애의 진행을 막는 정도의 치료가 이루어지고 있다. 본 연구를 바탕으로 소뇌 운동실조증으로 인한 운동질환(보행장애, 균형장애)과 흥분·억제 균형 이상으로 발생한 질환(안구운동 장애 등)에 대해 보다 적극적이고 근본적인 치료가 가능할 것으로 전망한다”고 밝혔다. 본 연구는 과학기술정보통신부(장관 유영민) 지원으로 한국연구재단 뇌과학원천기술개발사업, 리더연구자사업을 통해 수행되었으며, 연구결과는 미국 국립과학원 회보(PNAS, Proceedings of National Academy of Sciences, U.S.A.) (IF : 10.4, JCR 상위 : 5.469 % ) 최신호에 게재되었다. * (논문명) Control of motor coordination by astrocytic tonic GABA release through modulation of excitation/inhibition balance in cerebellum - (제 1 저자) 한국과학기술연구원 우준성 박사 - (교신 저자) 한국과학기술연구원 이창준 박사, 단국대학교 윤보은 교수 <그림설명> <그림 1> 소뇌에서 지속적 가바의 증가와 감소 지속적 가바의 분비의 채널을 담당하는 Best1이 결손된 마우스에서 지속적 가바가 현저히 감소됨을 확인하였고 (좌), 지속적 가바의 합성을 담당하는 효소인 MAOB가 별세포에서는 특이적으로 과발현되게 유도한 마우스에서는 지속적 가바가 증가함을 확인하였다 (우). <그림 2> 지속적 가바의 증가와 감소에 따라 조절되는 소뇌의 시냅스 전달 지속적 가바의 분비가 저해된 Best1 KO 마우스에서는 소뇌 신경세포의 발화 빈도가 증가해(붉은색 라인 증가) 신경전달이 원활하게 이루어졌고, 지속적 가바가 증가한 GFAP-MAOB 마우스에서는 반대현상이 나타나는 것을 소뇌의 MF-PC 시냅스 (좌) 및 PF-PC 시냅스에서 확인하였다.
- 23
- 작성자신경교세포연구단 이창준 박사팀
- 작성일2018.05.09
- 조회수16593
-
22
안정성을 유지하는 뇌의 비밀 밝힌다
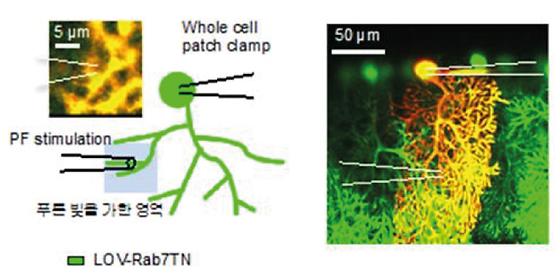
- 소뇌(cerebellum) 시냅스의 안정적인 학습 매커니즘 규명 - 새로운 광유전학 단백질로 다양한 뇌 부위 특성 연구에 활용 가능 소뇌(cerebellum)는 똑바로 걷거나 눈꺼풀, 눈동자가 움직이는 것과 같이 대뇌의 기능으로 이루어지는 근육운동을 세밀하게 만들고, 조화를 돕는 중요한 뇌 부위이다. 이러한 소뇌의 활동은 그 안에 존재하는 엄청난 양의 신경세포들 간 신호전달의 효율이 변화하고 그 변화를 유지하면서 일어난다. 최근 국내 연구진이 새로운 광유전학 단백질을 이용하여 신경신호의 효율 변화를 유지하는 뇌의 매커니즘 및 작동 타이밍을 규명했다고 밝혔다. 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 기능커넥토믹스연구단 게이코 야마모토 박사 연구팀(제1저자 김태곤 박사, 공동교신저자 유키오 야마모토 박사)은 일상적인 움직임의 미세조정과 운동학습을 담당한다고 알려진 뇌 부위인 소뇌(cerebellum)의 시냅스를 이용하여 소뇌의 학습 매커니즘을 규명하고, 시냅스의 신호 전달 효율의 변화 및 그 변화의 유지를 유발하는 스위치 체계를 발견했다. 시냅스(synapse)는 뇌세포끼리 신호를 전달하는 세포의 작은 부위이다. 시냅스에서는 자극의 세기, 반복 정도 등에 따라 신호의 전달 효율이 달라지고, 결국 똑같은 자극에 대해 정보처리 방식도 점점 달라지게 된다. 이 과정은 새로운 정보를 받아들여 학습하는 과정이고, 안정적인 학습을 위해서는 효율이 변화된 후 유지(장기간시냅스 억제/강화, long-term synaptic depression/potentiation)가 가능해야한다고 알려져 있다. 특히, KIST 게이코 박사팀은 세포내 수송경로(intracellular endosomal pathway)가 정보전달 효율의 변화와 유지의 핵심 기작으로 쓰인다는 그간의 가설을 증명했다. 또한 연구진은 변화한 효율의 유지를 유발하는 스위치 체계를 발견하여 소뇌 시냅스의 학습 매커니즘을 규명했다. 연구진은 푸른빛을 흡수하는 동안만 세포내 수송을 방해하는 새로운 광유전학 단백질 (LOV-Rab7TN)을 개발하였다. 먼저 전기적 자극을 가하여 시냅스억제 스위치를 작동시키고, 이 억제를 유지시키는 스위치가 켜질 것이라 예상되는 특정시점(억제 유도 후 약 15분 후)에 맞추어 빛을 가하여, 세포내 수송을 방해하는 광유전학 단백질을 활성화시켰다. 특정시점을 벗어난 푸른빛은 시냅스 정보전달 효율 변화에 아무런 영향을 미치지 못하고, 유지 스위치 작동시점에 맞추게 되면 성공적으로 시냅스억제를 중단시킬 수 있었다. 소뇌 시냅스는 효율 변화를 일으키는 자극에 항상 노출되어있지만, 변화 스위치와 유지 스위치가 순차적으로 작동하기 때문에 안정적인 학습이 가능해진다는 결론을 얻을 수 있었다. 연구진은 기존의 이론인 지속적으로 상태를 유지시켜주는 체계가 작동하는 것이 아니라 일시적인 스위치의 작동만으로도 시냅스가 안정적인 상태를 유지할 수 있다는 것을 밝혔다. 특히 이 순차적 스위치 체계는 세포내 수송체계를 통해 구현되고, 연구진이 개발한 광유전학 단백질을 통해 성공적으로 이를 조절할 수 있음을 보인 것이다. 순차적인 스위치 체계는 향후 다른 뇌 부위의 시냅스에도 적용하여, 빠르게 변화하면서도 안정적으로 정보를 처리하는 뇌의 독특한 특성을 설명하는 데 기여할 것이라 전망된다. 또한 연구과정에서 개발한 새로운 광유전학 단백질은 뇌세포 뿐 아니라 다른 종류의 세포내 수송체계에 대한 연구에도 광범위하게 적용가능하다. KIST 게이코 박사는 “소뇌에서 시냅스의 신호전달 효율의 변화를 유지하는 매커니즘을 밝히고 빛을 이용하여 이를 조절할 수 있다는 결과는 향후 움직임의 미세한 조정에 어려움을 겪거나 그런 조정을 학습하는 데 어려움을 겪는 환자들의 재활 등에 기여할 수 있을 것으로 전망한다.”고 밝혔다. 본 연구는 과학기술정보통신부(장관 유영민) 지원으로 KIST 기관고유사업 및 한국연구재단 중견연구자지원사업으로 수행되었다. 연구성과는 유명 과학저널인 ‘Nature Communications’ (IF: 12.124)에 9월 1일(금)자 온라인 게재되었다. <그림설명> <그림 1> LOV가 작동하는 방식 <그림 2> 실험 방식. 세포내 수송을 방해하는 Rab7TN을 LOV에 결합시켜 세포내에 발현하고 전기적으로 세포에 시냅스억제를 유도한 후 특정 시점에 푸른 빛을 가하여 세포내 수송을 방해함 <그림 3> 푸른빛을 특정시점 (시냅스 억제유도 후13-18분)에 가했을 때 억제되던 시냅스가 다시 제 위치로 돌아오는 상황 (붉은 동그라미)
- 21
- 작성자기능커넥토믹스연구단 게이코 야마모토 박사팀
- 작성일2017.09.07
- 조회수17849
-
20
저절로 춤추는 ‘무도병’, 새로운 치료기전 찾아
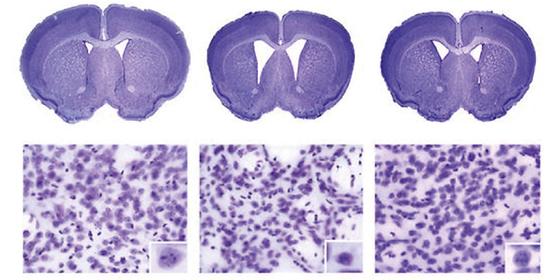
저절로 춤추는 ‘무도병’, 새로운 치료기전 찾아 - 퇴행성 뇌질환인 ‘헌팅턴 무도병’, 특정 효소의 조절로 신경세포 기능 회복 - 운동조절능력 향상과 수명 연장, 향후 퇴행성 뇌질환 치료에 기여 헌팅턴 무도병(Huntington’s chorea)이라고도 알려져 있는 헌팅턴병(Huntington’s Disease)은 유전적인 결함으로 뇌의 특정부위인 선조체의 신경세포에 광범위한 손상이 생겨 자신이 의도하지 않는 상태에서도 손과 발이 저절로 움직이는 퇴행성 뇌질환이다. 이 질병은 심각한 정신과적 증상과 더불어 나중에는 치매를 동반하는 것으로 알려져 있다. 뇌과학이 발달하기 이전의 중세에는 ‘춤추는 병(무도병)’에 걸린 사람들은 마녀사냥의 대상이 되어 화형에 처해진 경우도 있었다. 19세기, 이 ‘춤추는 병’은 의사 ‘조지 헌팅턴(George Huntington)’에 의해 부모로부터 자식에게 유전된다는 사실이 처음 발견되었고, 20세기에 들어 사람의 염색체 4번에 위치한 헌팅틴 유전자의 돌연변이(mutant Huntingtin)가 원인임이 밝혀졌다. 이후 춤추는 무도병, ‘헌팅턴병’에 대한 연구는 많이 이루어졌지만 아직까지 이 뇌질환을 호전시킬 약물이나 그 밖의 치료법은 전무했다. 한국과학기술연구원(KIST, 원장 이병권) 뇌의약연구단 류훈 박사연구팀(제1저자 이정희 박사, 황유진 박사, 김연하 박사, 이민영 박사, 현승재 박사과정)은 지난 15년간 헌팅턴병의 병리기전을 탐구하고 더불어 질병을 완화시킬 수 있는 약물 개발에 집중해왔다. 특히, 류훈 박사팀은 지난 연구에서 헌팅턴병 환자의 뇌 조직에서 ‘히스톤메틸화효소’의 증가에 따른 염색질의 응집 현상을 발견(*참고. PNAS 2006, Nucleic Acids Research 2014)한 바 있는데, 이번 연구를 통해 헌팅턴병 초파리 모델과 생쥐 동물모델에서 히스톤메틸화효소가 비정상적으로 증가하였을 경우 신경세포의 기능을 변화시키고 뇌의 병리와 운동조절에 이상을 일으키는 것을 밝혔다. 류훈 박사연구팀은 이 히스톤메틸화효소를 약물 타깃으로서의 가능성을 확인하고 헌팅턴병 생쥐모델에서 중개연구를 시행하였다. 흥미롭게도 비정상적으로 증가한 히스톤메틸화효소를 기존에 알려진 항생제 약물로 억제하면 히스톤메틸화의 항상성이 균형을 이루어 헌팅턴병 생쥐의 위축된 뇌의 선조체 신경세포의 기능이 회복될 뿐만 아니라, 운동조절능력의 향상과 수명이 연장된다는 사실을 밝혔다. KIST 류훈 박사는 “이번 연구는 헌팅턴병에서 보이는 신경세포의 손상과 행동장애를 완화시킬 수 있는 후성유전학적 치료제 개발의 가능성을 제시한다.”고 말하며, “이번 치료기전을 통해 다른 퇴행성 뇌질환인 치매, 파킨슨병과 같은 병리기전에 대한 이해와 치료에도 크게 기여할 것”이라고 밝혔다. 연구진은 실험에 사용한 항암제가 뇌질환 치료제로써 약효를 보이나 높은 농도에서 세포독성을 보이는 문제가 있어 향후 무해한 유사체 약물의 개발 등, 개선되어야할 점이 남아있다고 지적했다. 본 연구는 KIST 주도하에 미국 보스턴 의대와 공동연구로 진행하였으며, 미래창조과학부 지원으로 KIST 기관고유사업으로 수행되었다. 연구성과는 뇌병리 연구분야의 권위지로 알려진 ‘Acta Neuropathologica’ (IF : 11.360)의 PubMed 카테고리에 6월 7일(수)자 온라인 게재되었다. <그림설명> <그림 1> 히스톤메틸화효소를 약물(nogalamycin)로 조절한 결과, 헌팅턴병 생쥐의 선조체 신경세포(Striatal neurons) 핵 안에서 응집된 염색질 (빨강색)과 핵질 (파랑)이 다시 풀어져 분자적 변형이 복구되고 있음을 보여줌. <그림 2> 헌팅턴병 생쥐의 선조체 신경세포 위축(atrophy)되어져 있는데, 약물(nogalamycin)을 투여한 결과 신경세포의 크기가 회복되고 있음을 보여줌. <그림 3> 헌팅턴병 생쥐의 선조체 신경세포의 시냅스 구조 (주황색 화살표) 역시 위축되어 있는데, 약물(nogalamycin)을 투여한 결과 시냅스의 구조가 회복되고 있음을 보여줌.
- 19
- 작성자뇌의약연구단 류훈 박사팀
- 작성일2017.06.19
- 조회수28176
-
18
단백질 당화, 뇌 인지기능에 영향 미친다
단백질 당화, 뇌 인지기능에 영향 미친다 - 비정상적으로 증가된 단백질 당화와 학습능력 저하의 상관관계 규명 - 노화에 따른 당화 증가와 인지기능 저하 사이의 새로운 연결고리 제시 단백질에 일어나는 당화(오글루넥 糖化, O-GlcNAc glycosylation)*는 단백질의 기능을 조절하여 세포의 영양상태를 반영하는 신호전달체계로써, 세포의 영양상태 불균형에 따른 부적절한 당화는 현대인의 만성질환을 유발하는 원인으로 알려져 있다. 최근 국내 연구진이 단백질에 일어나는 오글루넥 당화가 비정상적으로 증가될 때, 신경 세포간의 결합세기의 유동성이 떨어지고 인지기능이 저하되는 것을 밝혔다. *오글루넥 당화(O-GlcNAc glycosylation): 단백질에 포도당 유도체인 ‘아세틸글루코사민’이 결합하는 것 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 임혜원 박사는 울산과학기술원(UNIST, 총장 정무영) 서판길 교수와의 공동연구를 통해 유전자 변형을 통해 오글루넥 당화를 인위적으로 증가시킨 실험 쥐의 경우 새로운 정보를 학습하는데 더 오랜 시간이 소요되며, 학습한 정보의 정확성도 떨어진다는 사실을 규명했다. 본 공동 연구진은 실험을 통해 일반적으로 새로운 정보를 습득할 시에 두뇌의 해마 부위에 위치한 신경세포간의 연결세기가 변화하는 과정이 필수로 일어나야 하지만, 당화가 증가된 유전자 변형 쥐에서는 외부에서 학습을 유발하는 자극이 주어졌을 때도 신경세포 간 연결의 세기가 유동적으로 변하지 않음을 증명했다. 오글루넥 당화는 포도당의 유도체가 단백질에 결합하여 일어나는 변화로써, 체내의 포도당 농도에 따라 민감하게 반응한다는 사실이 알려져 있으며 유전자의 발현이나 세포가 성장하여 분열하고 다시 성장하여 증식하는 세포주기 조절에 중요한 역할을 하는 것으로 학계에 보고된 바 있다. 본 연구는 오글루넥 당화와 학습능력 사이의 상관관계를 관찰하여 세포의 영양상태가 뇌 인지기능에도 영향을 줄 수 있음을 밝혔다는 점에서 큰 의미가 있다. 이번 연구 결과를 통해 KIST 임혜원 박사는 “치매와 같은 퇴행성 뇌질환뿐만 아니라, 노화 및 당뇨에서 흔히 발생하는 비정상적인 단백질 당화와 인지기능 저하 사이의 상관관계에 대해 추가 연구를 통해 더욱 면밀히 관찰할 필요가 있다” 고 말했다. 이번 연구는 미래창조과학부(장관 최양희) 바이오의료기술, 뇌과학원천기술개발사업 및 KIST 기관고유사업 지원으로 수행되었으며, 연구 결과는 ‘Scientific Reports’ 에 4월 3일(월)자 온라인 판에 게재되었다. <그림설명> <그림 1> 뇌단백질의 오글루넥 당화가 비정상적으로 증가된 유전자변형 쥐 모델에서 인지기능이 저하됨을 확인 <그림 2> 본 연구에서 사용된 다양한 행동실험에서 정상쥐 대비 Oga+/-쥐의 인지기능이 현저히 저하됨
- 17
- 작성자뇌과학연구소 임혜원 박사팀
- 작성일2017.04.06
- 조회수23049
-
16
신경 장애, 생체에 이식한 신경전극으로 치료한다
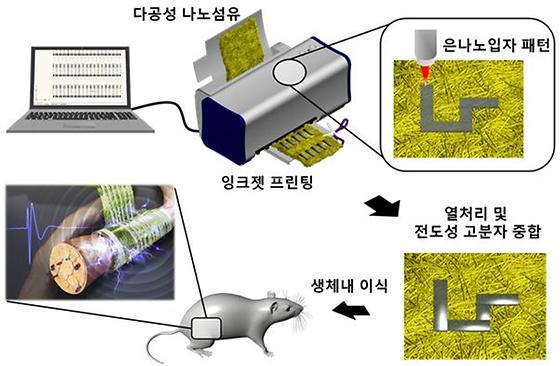
신경 장애, 생체에 이식한 신경전극으로 치료한다 - 생체 적합성이 우수한 나노섬유 기반의 생체이식형 신경전극 개발 - 신경장애 치료를 위한 신호 감지 및 제어시스템 연구에 기여 국내 연구진이 장기간 신경 자극에 의해 발생하는 신경 신호를 기록할 수 있는 안정하고 효율적인 생체이식형 신경전극 개발에 성공했다. 이 기술은 중추·말초 신경계 질병 및 손상에 의해 발생하는 신경장애의 치료를 위한 목적으로 사용되는 신경전극 기반 신경신호 감지 및 제어 시스템 연구에 도움이 될 전망이다. 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 바이오마이크로시스템연구단 이수현 박사팀은 경희대학교 치과재료학교실 권일근 교수팀, 건국대학교 수의과대학 도선희 교수팀과 공동연구를 통해 스펀지 형태의 다공성 나노섬유구조체 표면에 은 나노 입자를 잉크젯 프린팅 방식으로 전사한 신경 전극 개발에 성공했다. 연구진은 개발한 생체이식형 전극이 말초신경계의 신경 신호를 장기간 동안 안정적으로 측정 가능하다고 밝혔다. 최근 중추신경계와 말초신경계에서의 신경치료는 생체 신경 신호의 측정 및 자극이 가능한 이식형 신경 전극을 삽입하는 치료방법이 주목받고 있는데 주로 척추 손상 환자의 재활과 치료, 시신경 자극을 통한 인공 시각 구성, 정신적 질환의 치료를 위한 뇌 심부 자극술등의 치료 및 재활에 폭넓게 활용되고 있다. 그러나 기존 대부분의 이식형 신경 전극의 경우, 실리콘이나 고분자 필름을 하부구조로 제작되어 물질 투과성이 낮고, 체내에 이식이 된 후에 신경에 충분한 영양소 및 산소공급이 힘들며, 신경 조직에 비해 상대적으로 기계적 강도가 높아 이식부위에 기계적 부조화에 의한 상처가 발생하기 쉽다. 또한 체내에서 이물반응에 의한 염증으로 신경전극이 주변 조직과 차단되어 장기간 신경신호 검출이 어렵다는 한계가 있었다. 이에, 본 연구팀은 염증억제와 장기간 미세한 신경신호 검출을 위해서 신경전극의 유연성과 물질 투과성을 크게 향상시키면서 전기적으로 높은 감도를 갖는 신경전극을 개발하였다. 기존의 신경전극에 비해 월등히 향상된 유연성과 투과성을 갖기 위해서 나노섬유(Polyimide, 폴리이미드)를 이용하여 신경전극의 하부구조를 만들고, 그 위에 은 나노입자를 잉크젯 프린팅 방식으로 전사(Patterning, 패터닝)하였다. 그리고 전사된 은 나노입자 위에 전기적인 성능을 개선하기 위해서 전도성 고분자를 증착시켰다. 이렇게 제작된 신경전극은 체내 이식 후, 신경조직을 검사한 결과 신경 변형이나 위축 등 아무런 손상이 발생하지 않은 것을 확인하였다. 그 결과, 전기적 신호 감도가 뛰어나고 동시에 장기간 안정적인 신경 신호 기록이 가능한 신경전극을 개발할 수 있었다. 이수현 박사는 “본 연구로 개발된 신경전극은 장기간에 걸친 뛰어난 생체적합성을 검증받아 중추 및 말초신경계 손상의 신경계 장애인을 치료할 수 있는 안정적인 신경신호 검출과 기록이 가능하다. 또한 이 신경전극 개발에 적용된 기술은 각종 체내 삽입형 소자의 생체적합성을 향상시키는데 적용될 수 있다” 고 말했다. 본 연구는 미래창조과학부(장관 최양희)의 공공복지안전연구사업으로 “신경계 장애인의 신경신호 감지 및 제어 원천기술개발”과제(총괄과제책임자, KIST 강지윤 단장) 및 KIST 기관고유사업의 지원으로 이루어졌으며, 연구결과는 미국화학학회(ACS)에서 발간하는 세계적인 권위지인 나노 분야 국제학술지 ACS NANO (IF:13.334)에 2월 14일(화)자 온라인 판에 게재되었다. * (논문명) Flexible and Highly Biocompatible Nanofiber-Based Electrodes for Neural Surface Interfacing - (제1저자) 허동녕 박사, The George Washington University 포닥(前 경희대 박사) - (교신저자) 한국과학기술연구원(KIST) 이수현 박사(과제 실무책임자) 경희대학교 권일근 교수(세부과제 4, 공동연구자) 건국대학교 도선희 교수(위탁과제 연구(동물실험) <그림 설명> <그림 1> 다공성 나노섬유 기반의 유연한 성질의 신경전극 제작 과정 <그림 2> 잉크젯 프린팅 방식으로 제작된 다공성 나노섬유 기반의 신경전극 개념도
- 15
- 작성자바이오마이크로시스템연구단 이수현 박사팀
- 작성일2017.03.06
- 조회수18336
-
14
내 몸의 GPS, 공간과 상황을 인지하는 장소 세포의 매커니즘 규명
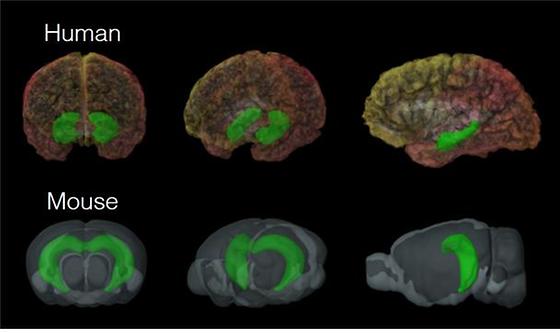
내 몸의 GPS, 공간과 상황을 인지하는 장소 세포의 매커니즘 규명 - KIST 뇌과학연구소 외국인 유치과학자, 장소 세포의 공간적, 감각적 기능 규명 - 트레드밀 활용 쥐 실험을 통해 물체에 대한 장소세포의 활동 기록·관찰 뇌의 해마(hippocampus)는 우리가 경험하는 사건을 기억하는데 필수적인 뇌 영역이다. 해마에 있는 각 세포가 우리가 있는 특정위치를 암호화하기 때문에, ‘장소 세포’(place cell)라고 일컫는다. 최근 국내 연구진이 내 몸 안의 GPS, 장소 세포에 대한 매커니즘을 규명했다. 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 세바스쳔 로열 박사(Sebastien Royer)는 KU-KIST 학연프로그램을 통해 고려대학교(총장 염재호) 심리학과 최준식 교수팀과 공동으로 공간과 사건/상황을 인지하고 기억하는 장소 세포의 기작(매커니즘)을 규명했다고 밝혔다. 해마라는 뇌의 부위에서 발견된 장소 세포는 장소를 인지하고 자기좌표를 파악하여 길 찾기에 도움을 주는 신경세포로 동물과 인간이 어떤 특정한 위치에 있는 경우만 발화하기 때문에 공간 좌표를 부호화한다고 알려진 신경세포이다. 해마의 장소 세포에 관한 연구는 2014년 노벨 생리학상을 수상한 바 있으며, 행동인지신경과학 분야의 첨단 주제로 알려져 있다. 본 연구진은 지금까지의 연구들이 모든 장소 세포가 같은 방식으로 공간정보를 기록하고 저장한다는 학설에 반해, 장소 세포는 공간적 정보와 비공간적(감각적) 정보를 집적하는 두 종류로 분명히 구분되며, 이들이 해마상의 해부학적 구조를 따라 상?하층으로 질서정연하게 배열되어 있음을 발견하였다. 본 연구에서는 실험용 쥐가 거칠거나 부드러운 바닥 혹은 튀어나온 돌기 등 다양한 촉각 단서가 부착된 트레드밀을 걷게 하면서 뇌의 신경활동을 기록하였다. 연구진은 실험용 쥐의 해마에 정교한 반도체 기판으로 이루어진 미세전극(실리콘 프로브)을 삽입하여 수십에서 수백 개에 이르는 장소 세포의 활동을 동시에 기록했다. 기록된 장소 세포들은 트레드밀 상에서의 위치를 부호화하는 방식에 따라 두 가지 유형으로 나뉘는데, 첫 번째 그룹은 기존의 장소 세포 이론에서 알려진 바와 같이 트레드밀 상의 특정 위치에서 발화하는 양상을 보였다. 두 번째 그룹은 트레드밀 상의 위치와는 상관없이 어느 특정 촉각 단서에 의존적으로 발화하는 양상을 보였다. 예를 들어 튀어나온 돌기 형상의 촉각 단서를 중심으로 발화하는 두 번째 그룹의 장소 세포의 경우, 그 촉각 단서를 제거하자마자 발화가 사라졌고 반대로, 트레드밀의 다른 위치에 똑같은 촉각 단서를 부착하기만 하면 즉시 유사한 발화 양상이 나타났다. 이러한 두 가지 유형으로 구분되는 장소 세포들의 발화 방식은 다양한 실험 조건에서 안정적으로 관찰되었다. -장소 세포 1그룹 : 공간적 위치 좌표를 인식하는 CM(context-modulated) 세포 -장소 세포 2그룹 : 주요 지형지물을 감각적으로 인식하는 LV(Landmark vector)세포 본 연구진은 세계 최초로 두 종류의 장소 세포들이 해마의 같은 영역에서 서로 다른 층(layers)을 따라 배열되어 있다는 것을 발견했다. 지금까지의 장소 세포 관련 연구들은 해마의 영역에 따른 수평적 분포에 집중하였으나, 본 연구진은 같은 영역에서 깊이에 따른 수직적 분포를 기능적으로 구분했다. KIST 세바스쳔 로열 박사는 “동물과 인간에서 기억의 핵심을 담당하는 해마가 장소와 관련된 추상적 정보를 어떻게 부호화하는지를 이해하는 데 한발 다가섰으며, 이러한 결과는 기억상실증이나 치매와 같은 기억 관련 질환들에서 망가진 신경회로를 대체할 수 있는 획기적인 방식을 발견하는 단서를 제공하고 새로운 인공지능 알고리즘을 제공하는 등 다양한 영역에 응용이 가능할 것”이라고 밝혔다. 본 연구는 휴먼프런티어 사이언스 프로그램, 미래창조과학부(장관 최양희)의 뇌 원천 연구사업 및 KIST 기관고유사업의 지원으로 이루어졌으며, 연구결과는 저명한 국제학술지인 네이쳐 커뮤니케이션즈 (Nature Communications, (IF : 11.329))에 2월 20일(월)자 온라인 판에 게재되었다. * (논문명) Place cells are more strongly tied to landmarks in deep than in superficial CA1 (Embargo:30 January 2017 at 1600 London time / 1100 US Eastern time ㅇddd30 January 2017 at 1600 London time / 1100 US Easte 1000 London time (GMT) / 0500 US Eastern Tim = 2월 20일(월요일) (한국시간 오후 7시) - (제1저자) Tristan Geiller - (교신저자) Sebastien Royer <그림 설명> <그림 1> (위) 인간 뇌와 (아래) 마우스 뇌 <그림 2> (좌) 해마의 신경회로, (우) 2가지 종류의 해마 장소세포들이 발화하는 양상 <그림 3> (좌) 촉각단서에 의존적인 장소세포가 단서가 제거되자 즉시 발화양상을 변화시키는 모양 (우) 반대로 촉각단서가 더해지자마자 새로운 발화양상이 출현하는 모양
- 13
- 작성자뇌과학연구소 세바스쳔 로열 박사팀
- 작성일2017.02.21
- 조회수20273
-
12
뇌 신경 회로망, 이제 실험실에서 배양한다
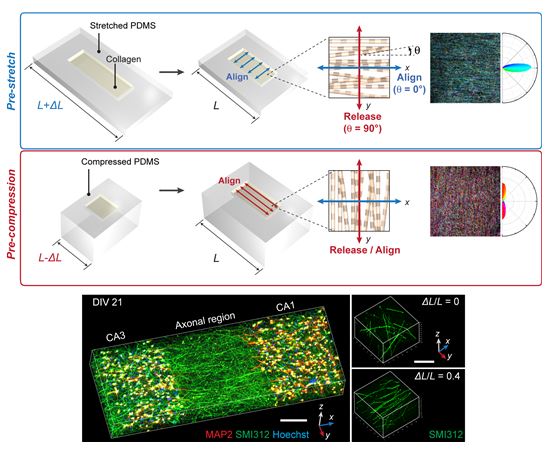
뇌 신경 회로망, 이제 실험실에서 배양한다 - KIST 뇌과학연구소, 뇌 신경망 재구성을 위한 3차원 플랫폼 개발 - 3차원 체외 환경에서 뇌 안에 있는 해마 신경 회로망의 구조 및 기능을 구현 최근 국내 연구진이 많은 신경 회로망들이 복잡하게 연결된 뇌 조직을 실제 세포 배양에 쓰이는 생체재료(3차원 체외환경) 내에서 구현하는 기술을 개발했다. 한국과학기술연구원(KIST, 원장 이병권) 뇌과학연구소 최낙원 박사, 허은미 박사 팀으로 구성된 공동 연구팀은 콜라젠 섬유를 특정 방향으로 정렬할 수 있는 기술을 세계 최초로 개발하여 콜라젠 내에서 신경세포를 3차원 배양할 때 세포 축삭*의 성장 방향을 유도할 수 있도록 하였다. *축삭 : 신경 세포(뉴런)의 세포체에서 길게 뻗어나온 가지로, 활동 전위를 전달하는 역할을 함. 축삭, 축색돌기, 축색이라고도 함 본 공동 연구팀은 이 기술을 적용하여 뇌 안에 있는 해마의 CA3, CA1**에서 추출한 신경세포들이 정렬된 콜라젠 섬유를 따라 분화, 성장하면서 시냅스를 형성하는 CA3-CA1 신경 회로망을 재구축하는데 성공하였다. 또한, 이 신경 회로망이 구조적 연결성뿐만 아니라 기능적 연결성도 갖추었음을 실험적으로 증명하였다. *CA3, CA1 : 대뇌변연계의 양 쪽 측두엽에 존재하는 해마 내 부위이며 학습과 기억을 담당 우리 몸 안의 여러 장기 및 조직은 세포와 세포 이외에 다양한 요소들이 흔히 특정 방향으로 정렬되어 있는데, 이것은 구조적인 속성을 부여하여 생물학적 기능이 작동되도록 하기 위한 것이다. 조직공학 측면에서 보자면, 체외 환경에서 장기 또는 조직을 새롭게 만들어 내고자 할 때 세포의 방향성을 구현하고 조절할 수 있다는 것은 조직의 외형적 구조뿐만 아니라 기능도 모사할 수 있다는 것을 의미한다. 본 연구 성과는 실제 세포 배양에 쓰이는 생체재료(3차원 체외 환경) 내에서 방향성 구현이라는 난제를 해결하고, 특히, 해부학적으로 뚜렷하게 구별되는 많은 신경 회로망들이 서로 복잡하게 연결된 뇌 조직을 체외환경에서 재구축했다는 것에 큰 의미가 있다. 이번 연구 결과를 통해 최낙원 박사는 “정상적인 신경 회로망뿐만 아니라 알츠하이머 병, 파킨슨 병 등 비정상적인 질병 상태의 신경 회로망까지 재구축하는 데 적용될 수 있다.”고 말했다. 또한, 허은미 박사는 “이번 기술을 환자 유래 줄기세포 기술과 융합한다면 다양한 뇌질환/장애와 신경 회로망의 기능 장애와의 연관성을 이해하는데 한 발짝 더 다가갈 수 있을 것”이라고 전망했다. KIST 뇌과학연구소 내 바이오마이크로시스템연구단 최낙원 박사와 신경과학연구단 / 치매DTC 융합연구단 허은미 박사 공동 연구팀은 UST(과학기술연합대학원대학교) 전공 교원으로 KIST 스타 포스닥 김소현 박사(현재 SK 바이오팜 재직), 임선경 박사(신경과학연구단/치매DTC융합연구단), 그리고 선임연구원 오수진 박사(신경과학연구단/치매DTC융합연구단/신경교세포연구단)와 함께 UST 학생을 포함하는 국내 연구자들로만 구성된 팀의 공동 연구를 통해 독자적으로 이루어낸 성과이기에 그 의미가 더욱 크다. 또한, Nature Communications 부편집자 Amos Matsiko 박사는 해외 리뷰 학술지인 Nature Reviews Materials에 이번 연구 결과를 Research Highlight(연구 하이라이트)로 2017년 2월 21일경 소개할 예정이다. 이번 연구는 미래창조과학부(장관 최양희) 뇌과학원천기술개발사업과 KIST Young Fellow 사업, 미래선도형융합연구단 사업의 지원으로 수행되었으며, 연구 결과는 저명한 국제 학술지인 네이쳐 커뮤니케이션즈 (Nature Communications, (IF : 11.329))에 2월 1일자 온라인 판에 게재되었다. * (논문명) Anisotropically organized three-dimensional culture platform for reconstruction of a hippocampal neural network - (공동 1저자) 김소현, 임선경, 오수진 - (공동 교신 저자) 최낙원, 허은미 <그림 설명> <그림 1> 해마 내 상이한 CA3, CA1 세포군을 구획화할 수 있도록 고안한 3차원 세포 배양 플랫폼 (위)에 신경세포를 배양하면, 축삭의 성장 방향을 일정하게 유도 (아래) <그림 2> 투명한 탄성 고분자인 PDMS 기판을 미리 당기거나 (pre-stretch), 눌렀다 (pre-compression) 놓으면서 콜라젠 하이드로젤을 굳히면, PDMS가 변형되었다 복원되는 방향과 직각 (파란색, 위) 또는 평행한 (빨간색, 중간) 방향으로 콜라젠 섬유가 일괄 정렬하게 되고, 이를 따라 정렬된 축삭의 구조가 서로 다른 뇌 부위를 기능적으로 연결하게 됨
- 11
- 작성자뇌과학연구소 최낙원 박사, 허은미 박사팀
- 작성일2017.02.13
- 조회수21374
-
10
KIST, 두 마리 토끼 잡은 알츠하이머병 신약물질 발굴
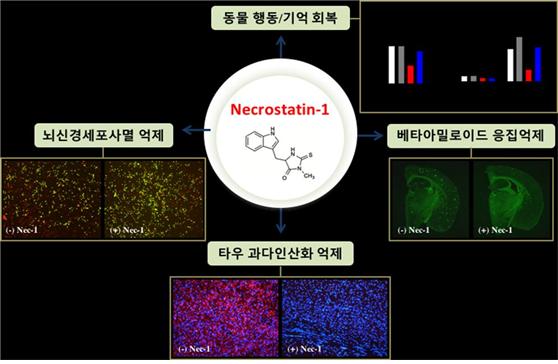
KIST, 두 마리 토끼 잡은 알츠하이머병 신약물질 발굴 - 주요 발병기전인 베타아밀로이드(Aβ), 타우(tau) 단백질을 동시에 표적억제 - ‘Necrostatin-1’신약물질 생쥐 투여 후 인지기능 정상 수준으로 회복 - 치매DTC 융합연구단 및 대통령 Post-Doc 펠로우십 사업 수행 성과 알츠하이머병(알츠하이머성 치매)은 현대인의 10대 사망 원인 질환 중 유일하게 예방 및 치료 방법이 없는 질병으로 치매의 60~80%를 차지하는 가장 흔한 퇴행성 뇌질환이다. 현재까지 알려진 알츠하이머병의 주요 특징은 뇌 속에 존재하는 베타아밀로이드와 타우 단백질 이상 현상으로, 이들을 각각 표적하는 약물이 개발된 바 있으나 연이은 임상실패로 인해 학계와 산업계 전문가들은 베타아밀로이드와 타우, 두 개의 학파로 나뉘어 어떤 단백질을 조절해야 알츠하이머 치료가 가능한지 20년 넘게 치열한 논쟁을 벌이고 있었다. 한국과학기술연구원(KIST, 원장 이병권) 치매DTC융합연구단 김영수, 양승훈 박사팀은 베타아밀로이드와 타우 단백질의 이상 현상을 동반 억제하는 신약 후보물질인 Necrostatin-1(네크로스타틴-원)을 개발했다. 이 합성신약은 동시에 두 단백질을 직접 뇌에서 조절하고, 치매 증상을 정상 수준으로 회복시켜줄 수 있는 물질로, 국제적으로 처음 보고되는 치료방법이다. 알츠하이머병은 환자의 뇌에서 베타아밀로이드의 집적으로 인해 나타나는 신경반과 타우단백질의 과다인산화/집적으로 인해 나타나는 신경섬유다발의 형성이 주요 특징으로 관찰되고 있다. KIST 김영수 박사, 양승훈 박사팀은 Necrostatin-1(네크로스타틴-원)이라는 신약 후보물질을 알츠하이머 생쥐에 투약하였을 때, 베타아밀로이드 단백질의 응집체가 뇌에서 현저하게 감소되며, 타우 단백질의 과다인산화 및 응집현상 역시 억제된다는 기능을 밝혀내었다. 알츠하이머병 주요 원인 단백질을 모두 표적 억제하기 때문에, 뇌세포 사멸을 억제시키고 인지기능이 개선되는 효능을 나타내었다. 연구진은 알츠하이머병 환자의 뇌세포가 점점 죽어가면서 뇌의 크기가 작아지고 인지능력도 줄어든다는 사실에 집중해 뇌세포자연사와 괴사를 모두 억제할 수 있는 약물(Necrostatin-1)을 연구 중이었다. 연구 중 Necrostatin-1 (네크로스타틴-원)이 베타아밀로이드 응집현상을 조절하며, 뿐만 아니라 타우단백질의 과다인산화 및 응집을 억제한다는 사실을 밝혀냈다. 연구진은 이 결과를 바탕으로 네크로스타틴-1을 알츠하이머병에 걸린 생쥐에게 3개월간 투여한 후 뇌기능의 변화를 관찰했고, 인지 능력을 관장하는 뇌의 해마와 대뇌피질 부위에 있는 베타아밀로이드 응집체 및 타우단백질 과다인산화가 모두 제거된 것을 발견했다. 생쥐의 기억력 검사인 행동시험(Y-maze, Passive avoidance)에서 약물이 투여된 알츠하이머 생쥐의 인지 기능이 정상 수준으로 회복된 것을 알 수 있었으며, 또한, 알츠하이머병이 진행되면 나타나는 뇌 신경세포의 사멸 및 뇌 구조의 파괴 등의 증상 역시 사라짐을 확인했다. 이번 연구결과는 베타아밀로이드 및 타우를 각각 별개로 억제시키는데 초점을 맞춘 기존의 치료제 개발방법과 차별된다. 개발된 네크로스타틴-1은 병의 증상과 함께 나타나는 뇌신경세포사멸 기전 조절을 통한 새로운 치료방법이며, 베타아밀로이드와 타우 단백질을 동시에 조절할 수 있는 획기적인 신약후보물질이다. 김영수 박사는 “이번 연구 성과는 국제적으로 오랜 논쟁의 대상인 ‘아밀로이드 vs 타우’ 가설의 종지부를 찍을 수 있는 새로운 치료전략을 제시했다는 것에 의미가 크다.”며, “본 연구의 결과를 토대로 알츠하이머병의 병리학적 원인 규명 및 근원적 치료제 개발 연구에 더욱 힘쓸 예정”이라고 말했다. 또한, 양승훈 박사는 “세포자연사(apoptosis)와 괴사(necrosis)가 합쳐진 개념인 네크롭토시스(necroptosis)가 뇌질환에 미치는 영향을 광범위하게 연구 중이다”라고 밝혔다. 연구진은 이번에 개발된 신약물질을 의약품으로 허가될 수 있도록 전임상 및 임상 연구를 추진하고 있으며, 또한 알츠하이머병의 혈액 진단 시스템 개발 사업과 연계되어 알츠하이머병의 진단과 치료를 동시에 수행할 수 있는 연구도 진행 중이다. 본 연구는 국가과학기술연구회(NST, 이사장 이상천) 치매DTC융합연구단(단장:배애님 박사/KIST) 및 교육부(장관 이준식, 전담기관:한국연구재단) 대통령 Post-Doc 펠로우십 지원을 통해 수행되었다. 본 연구 결과는 세계적으로 권위있는 과학지인 ‘EMBO Molecular Medicine’(IF:9.5, JCR:5.6%)에 11월 17일자로 온라인 게재되었다. <그림자료> <그림 1> 신약후보물질의 알츠하이머병 치료 효과 (베타아밀로이드 응집), 치매 생쥐 뇌(좌), 약물 투약 후 치매 생쥐 뇌(우) 알츠하이머병이 유발된 생쥐 모델에 네크로스타틴-1을 투여한 결과 병을 유발하는 좌측사진의 점으로 보이던 베타아밀로이드 응집체가 뇌에서 모두 사라졌음. <그림 2> 신약후보물질의 알츠하이머병 치료 효과 (타우 과다인산화), 치매 생쥐 뇌(좌), 약물 투약 후 치매 생쥐 뇌(우) 알츠하이머병이 유발된 생쥐 모델에 네크로스타틴-1을 투여한 결과, 병을 유발하는 좌측 사진의 붉은 점의 타우단백질 과다인산화가 뇌에서 모두 사라졌음. <그림 3> 신약후보물질의 알츠하이머병 치료 (종합) 알츠하이머병의 원인 독성 단백질인 베타아밀로이드와 타우과다인산화를 완벽히 제거하고 인지 능력을 정상 수준으로 회복
- 9
- 작성자치매DTC융합연구단 김영수, 양승훈 박사팀
- 작성일2016.11.21
- 조회수25940
-
8
치매 전문가, 색다른 도전으로 뇌종양 치료에 변이와 내성 없는 신약 타겟 찾았다
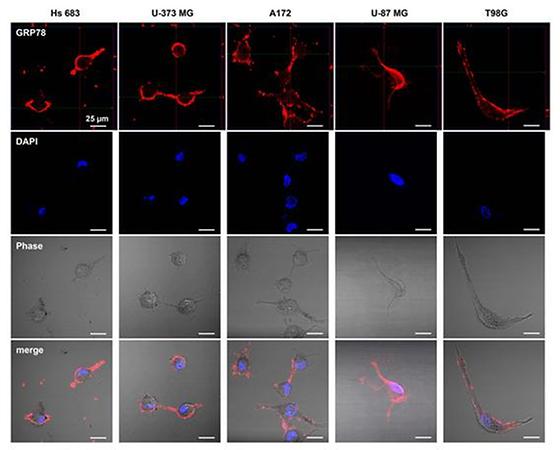
치매 전문가, 색다른 도전으로 뇌종양 치료에 변이와 내성 없는 신약 타겟 찾았다 - 단백질 ‘GRP78’*이 암 세포표면으로 이동하는 특이적 행동 규명 - 암 세포표면의 ‘GRP78’ 표적 시, 동시에 뇌종양의 전이억제와 치료가능 *단백질 ‘GRP78’ (포도당조절단백질(Glucose Regulated Protein 78 kDa)) : 분자량 78,000 포도당제어성 단백질 표적 항암치료제 ‘글리벡’은 정상세포에는 없고 암세포에만 있는 특이 유전자 변이를 찾아내고 암의 전이를 억제하는 "마법의 탄환(Magic Cancer Bullet)"이다. 하지만, 암세포가 새로운 유전자 변이를 만들 경우 내성이 생기고 표적항암제는 결국 무력화 되는 치명적인 단점이 있었다. 최근 KIST 연구진이 기존 표적항암제의 단점을 극복할 수 있는 획기적인 항암 치료전략을 개발했다. 한국과학기술연구원(KIST, 원장 이병권) 치매DTC융합연구단 김영수 박사팀은 뇌종양 발생 시, 평상시 세포 내부에만 존재하던 단백질 ‘GRP78’이 암세포표면으로 이동하여 과발현되며, 암의 전이를 조절하는 것을 세계 최초로 규명하였다. 연구진은 단백질 ‘GRP78’을 억제할 경우 뇌종양의 치료가 가능하다는 연구결과를 발표했다. 김영수 박사는 기존에 ‘혈액기반 치매진단시스템 개발’ 및 치매에 대한 괄목할만한 성과로 세간의 주목을 받았던 치매 전문가다. 김 박사는 치매 연구를 하는 동시에, 자율성을 보장, 색다르고 도전적인 연구를 위해 수행되는 KIST 기관고유사업 ‘KIST Young Fellowship’ 프로그램에 참여했다. 단순한 호기심에 의해 시작한 연구가 새로운 분야를 발굴하여 이와 같은 성과를 내었다. 연구팀은 임상 데이터 분석과 생쥐모델 연구를 통해 정상 뇌조직에 비하여 뇌종양 부위에서 단백질 ‘GRP78(Glucose Regulated Protein 78 kDa)’이 특이하게 과발현 되어있다는 점에 주목했다. 다양한 뇌종양 세포막을 분석한 결과, 신규 단백질의 접힘(Folding, 고유의 2차구조의 배치순서로 중첩을 통한 고차구조 형성)을 조절하는 열충격단백질(Heat Shock Protein, 열충격에 의해 합성이 유도되는 단백질)의 일종인 ‘GRP78’은 정상세포 내부에만 존재한다고 알려져 있었으나, 특이하게 뇌종양 암세포의 표면으로 이동하여 비이상적으로 발현된다. 연구진은 단백질 ‘GRP78’이 단순히 암세포를 정상세포로부터 구분하는 표지인자 역할 뿐만이 아니라, ‘GRP78’을 항체로 표적하여 억제 할 경우 암의 치료가 가능하다는 것을 밝혀냈다. 가장 흥미로운 점은, ‘GRP78’은 변이가 없다는 점이다. 암 특이성이 유전자 변이가 아닌 암세포막 발현 여부이기 때문에 유전자 변이에 의한 내성 문제를 피해갈 수 있다. 김영수 박사는 이번 연구를 통해 “단백질 ‘GRP78’은 전이가 되는 암의 표지인자이자 치료인자이다. 즉, 뇌종양의 전이억제와 치료가 동시에 가능하다. 특히 변이가 없기 때문에 내성이 없는 항암제의 개발을 전망하고 있다. 또한, 뇌종양은 대표적인 전이 암으로, 다른 종류의 전이 암도 ‘GRP78’ 표적항암전략으로 치료 가능할 것으로 예측하고 있다”고 말했다. 본 연구 결과는 세계적인 우수 과학 저널인 ‘Scientific Reports’에 10월 7일(금) 온라인 게재되었다. <관련자료> <그림1> 뇌종양에서의 GRP78 과발현 A) 임상 데이터, B) 세포 실험, C) 생쥐모델 실험을 통해 뇌종양 특이적으로 GRP78이 과발현 되는 점을 확인함. <그림 2> 뇌종양 세포 표면에 발현된 GRP78 정상세포에서는 세포 내부에만 존재하는 GRP78이 전이성이 높은 다양한 뇌종양 세포의 표면에 과발현 됨.
- 7
- 작성자치매DTC융합연구단 김영수 박사팀
- 작성일2016.10.13
- 조회수20253